Description de l'élevage
L'élevage naisseur engraisseur possède 1000 truies et est situé en Italie dans une zone à forte densité porcine. Les porcs arrivent à l'abattoir à 168 kg avec au moins 9 mois d'âge selon les règles de production du Consorzio del Prosciutto di Parma e San Daniele.
L'exploitation produit son propre renouvellement de cheptel avec un noyau de grand parentales. La conduite est en bande à la semaine et le sevrage est à 21 jours. On utilise la conduite en tout plein tout vide autant en sevrage qu'en engraissement. D'autre part, la capacité du local de croissance qui reçoit les animaux entre 20 à 40 kg a 5% de moins de capacité que les sevrages, ce qui signifie que les salles ne se mélangent pas entre elles.
Les deux salles ont un sol en caillebotis plein. Dans l'engraissement, où les animaux entrent à 40 kg, le sol est plein et les animaux sont répartis dans plusieurs salles d'engraissement. L'aliment au sevrage est à sec et à volonté alors qu'en phase de croissance et d'engraissement, il est liquide, administré 3 fois par jour.


Etat sanitaire
L'élevage est positif en SDRP, Aujeszky, Mycoplasma Hyorhinis et PCV2 et négatif en entérite nécrotique et rhinite atrophique.
Programme de traitement et de vaccination des reproducteurs : vaccination de masse 3 fois par an contre le parvovirus, l'Aujeszky et le SDRP. Les petites truies sont aussi vaccinées contre le mycoplasme. Tous les reproducteurs sont traités 3 fois par an à l'ivermectine dans l'aliment.
Porcs : la vaccination contre le mycoplasme est unique et celle contre l'Aujeszky est administrée à 60, 85 et 170 jours de vie. Le traitement pour le contrôle de la colibacillose et la streptococcie à l'entrée au sevrage est composé d'amoxicilline (400 ppm), de colistine (200 ppm).Pendant la phase de croissance, ils ne sont pas vaccinés.
Aparrition du cas
Les porcelets étaient normaux pendant le sevrage avec des pertes modérées (2%), mais après 15 à 20 jours de transfert, en phase de croissance, on notait l'apparition d'une toux généralisée et une perte de poids. La mortalité était de l'ordre de 30% et la mortalité de 4 à 6%. Cette situation était pratiquement chronique en phase de croissance et on l'avait toujours attribuée à une recirculation du SDRP. Après la phase de croissance c’est à dire en engraissement, les problèmes étaient de type entérique, avec une certaine mortalité mais dans les limites normales de l'exploitation (3%).

Visite de l'élevage
On a vérifié ce que l'éleveur avait relaté. On a noté aussi en phase de croissance, ce qui a motivé l'appel, la présence de quelques cas de diarrhées noires mais pas très étendues. La toux était présente chez des animaux âgés de 75-95 jours avec quelques prostrés avec un état fébrile. Pendant la visite, on n'a pas trouvé d'animaux morts.
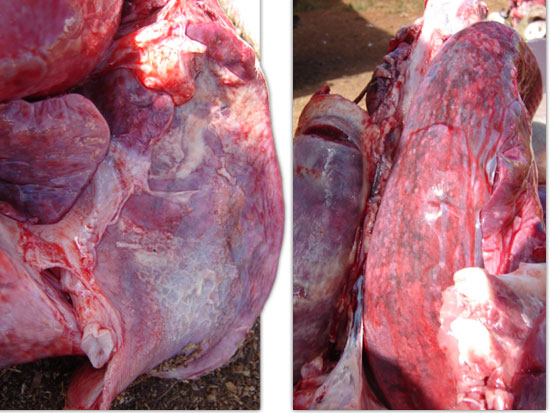
Photos 2 et 3: Pneumonie accompagnée de pleurésie
On a demandé à l'éleveur d'appeler si des animaux morts apparaissaient pour faire une autopsie, ce qui arriva quelques jours plus tard. A l'autopsie, on a mis en évidence une broncho-pneumonie avec présence de lésions compatibles avec du mycoplasme, une pneumonie interstitielle et une pleurésie diffuse avec des symptômes de complications bactériennes. On a envoyé les poumons au laboratoire pour déterminer les agents responsables. La suspicion était le SDRP avec complication bactérienne. L'élevage réalisait des analyses semestrielles par classe d'âge pour observer les variations possibles de la dynamique d'infection des virus en circulation dans l'élevage, le SDRP et le PCV2, qui produisent souvent des baisses de rendement. Parallèlement, on a effectué une analyse sérologique d'un groupe d'animaux, 8 par chaque tranche d'âge : 6, 9, 14, 20 et 26 semaines avec pour objectif d'identifier le moment où se produit la virémie. Selon le résultat du laboratoire, on a recommandé l'utilisation d'un antibiotique (chlortétracycline 200 ppm) et d'un anti-inflammatoire (paracétamol 600 ppm). Pendant la visite, on a effectué l'autopsie d'un animal mort subitement en engraissement au poids vif de 80 kg, qui a mis en évidence des altérations de type nécrotique dans la paroi du côlon.

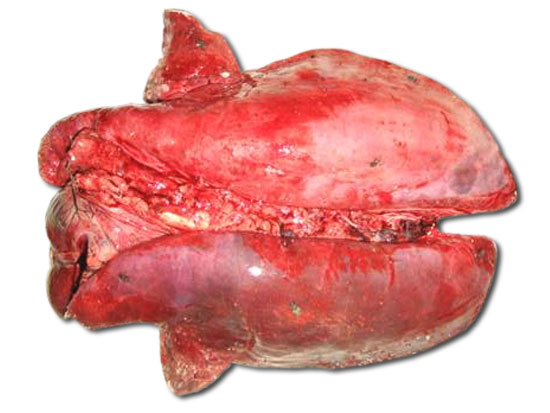
Tableau 1. Analyses sérologiques
| N° animaux |
Age (semaines) |
Présence |
SDRP PCR (+) 2 pool de 4 |
PCV2 PCR (+) 2 pool de 4 |
Mycoplasma Elisa (+) |
| 8 | 6 | Non | 2/2 | 0/2 | 0/8 |
| 8 | 9 | Oui | 2/2 | 2/2 | 4/8 |
| 8 | 14 | Oui | 2/2 | 2/2 | 1/8 |
| 8 | 20 | Oui | 0/2 | 2/2 | 7/8 |
| 8 | 26 | Oui | 0/2 | 2/2 | 6/8 |
R ésultats de laboratoire
- Analyses bactériologiques : isolement de Salmonella cholerasuis des poumons et de l'intestin et présence de Brachyspira pilosicoli dans l'intestin
- Analyse virologique : positif SDRP (PCR) et circovirus (PCR)
- Antibiogramme : sensible à l'aminosidine, la fluméquine, la gentamycine, l'amoxicilline.
Mesures adaptées
Avec le diagnostic de laboratoire et les observations de terrain, on décide de traiter tous les animaux en phase de croissance à l'aminosidine (12,5 ppm) dans la soupe contre la salmonellose pendant 15 jours.
Pendant le vide sanitaire on a nettoyé aussi les fosses, chose qui n'était pas faite auparavant. UnE fois propres, on a saupoudré de la chaux vive (qui a été tout de suite éteinte). Chaque salle est restée vide pendant 40 jours.
Traitement et évolution
Après presque deux semaines, on n'a observé aucune amélioration et, par conséquent, on a décidé de traiter dans la soupe avec de la fluméquine (600 ppm et de la tiamuline (100 ppm). L'utilisation d'aliment liquide rend difficile la séparation des animaux en groupe, c'est pourquoi on a décidé de traiter toute la phase de croissance.
Après presque 3 mois, on décide de réaliser le traitement seulement dans la première phase de croissance (15-20 jours), en laissant la seconde moitié sans traitement (les autres 15-20 jours). Après quelques semaines, cette action s'est montrée négative avec une réapparition de symptômes cliniques ; on a donc repris la médication pendant toute la croissance. Cette stratégie a impliqué une amélioration générale des performances (croissance, conversion alimentaire et mortalité) qui a continué jusqu'au jour d'aujourd'hui, même si les virus du SDRP et du PCV2 continuaient à être présents en phase de croissance. Pour le moment, on n'a pas isolé plus de souches de Salmonella cholerasuis et la symptomatologie ne s'est pas représentée.
Commentaire
- Malgré la présence de la circulation virale du SDRP et du circovirus concomitante au problème sanitaire, la mortalité et les retards étaient dus à l'infection secondaire par Salmonella.
- On n'a pas suspecté immédiatement Salmonella à cause du manque de symptomatologie intestinale évidente : le problème était de type respiratoire. Le genre cholerasuis de Salmonella est très invasif et circule facilement. Dans ce cas, il n'avait pas colonisé l'intestin de façon importante. Autre symptôme typique, la cyanose n’était pas non plus présente.
- Aujourd'hui, l'élevage continue le protocole de nettoyage et de désinfection de l'environnement et des fosses (chaux) pendant les vides de chaque salle.
Conclusions
- La présence constante de circulation du SDRP peut entraîner à sous-estimer d'autres agents pathogènes qui peuvent être la vraie cause de mortalité.
- La dose et la continuité du traitement doivent être soigneusement évaluées.
- Le « retour » de la maladie n'a pas à impliquer un arrêt immédiat du traitement.





